Đa xơ cứng là một bệnh tự miễn thường gây suy nhược đặc trưng bởi yếu cơ, vấn đề về thị lực, phối hợp suy yếu và tê vật lý. Hiện nay, phương pháp điều trị cho bệnh này tập trung vào việc quản lý các triệu chứng, nhưng nếu chúng ta có thể giải quyết nguyên nhân chính của chúng trong não?
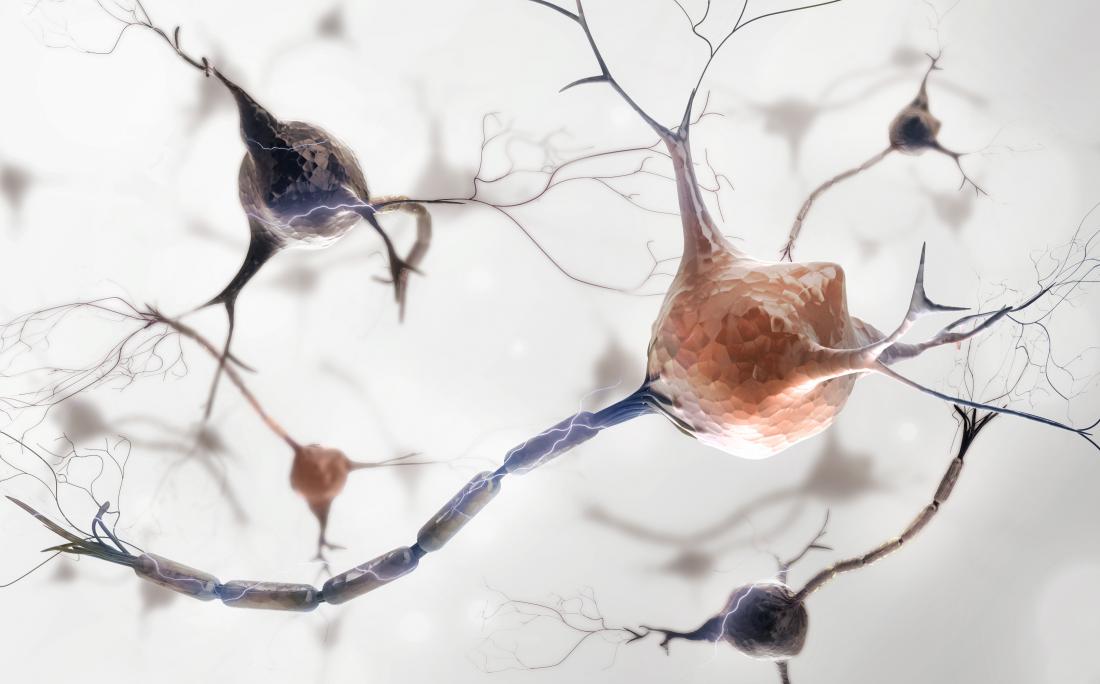
Mặc dù nguyên nhân gốc rễ của bệnh đa xơ cứng (MS) vẫn chưa được biết, chúng ta biết rằng một yếu tố cho các triệu chứng của nó là thoái hóa.
Trong quá trình này, hệ thống miễn dịch tấn công và phá hủy myelin, hoặc “phủ” xung quanh các sợi trục, đó là những dự đoán kết nối các tế bào thần kinh trong não và tủy sống.
Kết quả của sự hư hại này, tín hiệu truyền giữa các tế bào thần kinh bị gián đoạn, do đó các vấn đề về thị giác, phối hợp hoặc kiểm soát cơ bắp. Do đó, thách thức chính đối với các nhà nghiên cứu chuyên về MS là làm thế nào để thúc đẩy sự tái tổ hợp, đó là việc tạo ra một “vỏ bọc” myelin mới một cách hiệu quả và hiệu quả.
Theo một nghiên cứu năm 2016, hơn 403.600 người ở Hoa Kỳ sống với MS, trong khi một nghiên cứu trước đó chỉ ra con số ước tính khoảng 2,3 triệu người được chẩn đoán mắc bệnh trên khắp thế giới.
Tiến sĩ Veronique Miron – tại Trung tâm Nghiên cứu MS của Anh ở Anh, và các nhà khoa học khác đã thực hiện một bước đột phá trong nghiên cứu hồi phục khi họ phát hiện ra rằng một loại protein được gọi là activin-A đóng một vai trò quan trọng trong việc thúc đẩy sửa chữa myelin.
Vào thời điểm đó, họ không thể xác định được cơ chế nhờ đó mà protein tăng cường myelination. Nhưng bây giờ, Tiến sĩ Miron và nhóm nghiên cứu đã phát hiện ra loại protein này “chuyển mạch” như thế nào trong quá trình sửa chữa.
Các phát hiện của các nhà nghiên cứu đã được công bố trên tạp chí
‘Khuyến khích các tế bào tạo ra myelin mới’
Tiến sĩ Miron và các đồng nghiệp đã nghiên cứu cơ chế sản xuất myelin trong đó activin-A liên quan đến cả in vivo (sử dụng mô hình chuột của MS) và in vitro (trên mô người do Ngân hàng Mô tế bào cung cấp).
Các nhà khoa học nhận thấy rằng các quá trình dẫn đến việc sản xuất myelin phụ thuộc vào sự biểu hiện của thụ thể activin-A được gọi là receptor activin 2a (Acvr2a) trên oligodendrocytes, một loại tế bào có thể tạo ra myelin.
Nhìn vào các mẫu mô được hiến tặng bởi những người đã sống với MS tiến triển, tiến sĩ Miron và nhóm của bà thấy rằng mức Acvr2a cao hơn đáng kể trong các mô thần kinh được hưởng lợi từ việc hồi phục. Ngược lại, mức độ Acvr2a giảm trong mô mà không có dấu hiệu sửa chữa myelin.
Activin-A, các nhà nghiên cứu cũng phát hiện, liên kết với Acvr2a, báo hiệu các oligodendrocytes để bắt đầu công việc sửa chữa tại các vị trí mà vỏ myelin của sợi trục đã bị hư hại.
“Khi chúng tôi lần đầu tiên phát hiện ra protein này activin-A,” Tiến sĩ Miron lưu ý, “chúng tôi không biết chính xác vai trò của nó trong quá trình tái tổ hợp. Chúng tôi biết nó liên kết với một thụ thể cụ thể, mà sau đó gây ra các tế bào thực hiện sửa chữa myelin . “
Như remyeliantion là rất quan trọng để làm chậm sự tiến triển của bệnh và có khả năng ngăn chặn nó hoàn toàn, Tiến sĩ Miron nói rằng những phát hiện của nghiên cứu hiện tại cuối cùng có thể dẫn đến một mục tiêu ma túy mới.
“Đây là một khám phá thực sự thú vị bởi vì [chúng ta] bây giờ có thể tập trung nỗ lực vào việc phát triển các loại thuốc nhắm vào thụ thể. Nếu chúng ta có thể làm điều đó, chúng ta có thể khuyến khích các tế bào tạo ra myelin mới sau khi tổn thương đã được thực hiện trong MS.”
Tiến sĩ Veronique Miron
Dưới đây, bạn có thể xem một video trong đó Tiến sĩ Miron giải thích sự liên quan của những phát hiện của nghiên cứu trong điều trị MS, và cách họ có thể chỉ ra cách để điều trị tốt hơn, hiệu quả hơn.